Высокая щелочность пивоваренной воды не позволяет многим домашним пивоварам делать хорошее легкое пиво собственного производства. Чтобы это преодолеть многие используют воду из обратного осмоса, для разбавления имеющейся воды или даже для создания своей пивоваренной воду с нуля путем добавления солей. Другим вариантом является использование кислот для нейтрализации некоторой или всей щелочности воды.
Если щелочность всей воды или наибольшая ее часть является результатом временной жесткости (содержание растворенного карбоната кальция и магния), то существуют другие способы, которые обычно игнорируются. Одним из таких способов является осаждение щелочности гидроксидом кальция (также известного, как гашеная известь). Из-за низкой стоимости этот метод водоочистки широко применим в пивоваренной промышленности, но домашние пивовары, похоже, в большей степени остались в стороне из-за недостатка понимания химии и отсутствия поддержки в виде калькулятора.
Основываясь на данных в технической пивоваренной литературе, я смог заставить этот способ работать в моей воде и добавить необходимые вычисления в электронную таблицу расчета воды (водный калькулятор.xls). Данная статья пытается пролить свет на этот процесс и обеспечить наилучшее понимание химии, чтобы позволить другим пивоварам пользоваться этим элегантным способом очистки воды в их пивоваренном процессе.
Объяснение непонятной концепции
В большинстве пивоваренных книг упоминается, что щелочность и жесткость воды могут быть снижены при добавление извести (гидроксида кальция), которая сама по себе является сильной щелочью. Как может добавляться сильнощелочное соединение, такое как гашенная известь, для уменьшение щелочности? Это меня всегда запутывало, и мне потребовалось некоторое время, пока химия, стоящая за этим процессом, не стала для меня более понятной.
Гидроксид кальция является сильным основанием и, как таковой, он диссоциирует на кальций и гидроксид, когда растворяется в воде, независимо от рН воды:
- Ca (OH) 2 → Ca 2+ + 2 OH -
Образовавшиеся гидроксидные ионы (OH - ) стремятся повысить рН раствора, и в чистой воде это будет очень эффективно. Тем не менее, вода, которую мы обрабатываем известью, содержит бикарбонат и угольную кислоту, действующие как буфер рН и тем самым способствующие сильному повышению рН. Хотя мы наблюдали щелочность только в качестве препятствия для снижения рН затора, pH-буфер работает в обоих направлениях. Т.е. он удерживает рН от падения также, как он удерживает его от роста.
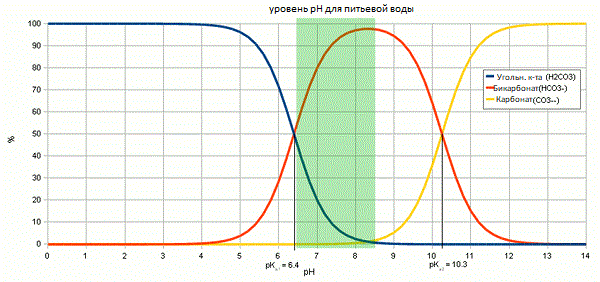 Рисунок 1 - Относительная концентрация угольной кислоты, бикарбоната и карбоната основанная на рН раствора. Для питьевой воды рекомендуется рН от 6,5 до 8,5
Рисунок 1 - Относительная концентрация угольной кислоты, бикарбоната и карбоната основанная на рН раствора. Для питьевой воды рекомендуется рН от 6,5 до 8,5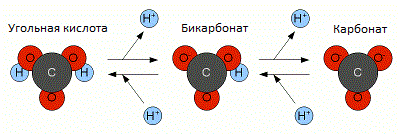 Рисунок 2 - Превращение угольной кислоты в карбонат через бикарбонат и обратно в угольную кислоту
Рисунок 2 - Превращение угольной кислоты в карбонат через бикарбонат и обратно в угольную кислотуПоскольку соотношение угольной кислоты, бикарбоната и карбоната находится в тесной связи с рН раствора (рис. 1), гидроксидные ионы извести должны взаимодействовать с угольной кислотой (H 2 CO 3 ), диоксидом углерода (CO 2, который не сформировал еще угольную кислоту) и бикарбонатом (HCO - 3 ) , чтобы увеличить концентрацию карбоната (CO 2- 3 ) с помощью следующих реакций
- CO 2 + OH - → HCO - 3
- H 2 CO 3 + OH - → HCO - 3 + H 2 O
- HCO - 3 + OH - → CO 2 - 3 + H 2 O
Добавленный гидроксид в основном притягивает ионы водорода (H + ) как из угольной кислоты, так и из бикарбоната, чтобы сделать их карбонатом. Это движение показано справа на рис. 2. В какой-то момент большая часть ионов гидроксида была поглощена вышеупомянутыми реакциями, а баланс угольной кислоты / бикарбоната / карбоната таков, что он сильно смещен в сторону карбоната. Это произошло с повышением рН, поскольку соотношение между рН и угольной кислотой / бикарбонатом / карбонатом, которое показано на рисунке 1, должно оставаться удовлетворительным.
Но для нас важно не повышение рН, а повышение концентрации карбонатных ионов. На этом этапе мы должны рассмотреть уравнение растворимости для карбоната кальция:
- [Ca 2+ ] * [CO 3 2- ] ≤ K sp = 3,36 × 10 -9
Если величина между концентрацией ионов кальция и карбоната больше 3,36 × 10 -9, что очень мало, тогда карбонат кальция будет выпадать из раствора в осадок до тех пор, пока концентрация кальция или карбоната не будет достаточно низкой, чтобы удовлетворить этому уравнению. Когда это осаждение происходит, то молочно-белое помутнение, состоящее из форм карбоната кальция (мела), медленно выпадет в осадок.
- Ca 2+ + CO 3 2- → CaCO 3 ↓
Стрелка вниз (↓) означает, что образовавшийся мел осаждается. Этот осаждающий мел представляет собой временную жесткость воды, а оставшаяся прозрачная вода имеет более низкую щелочность и более низкую жесткость (т.е. меньшее содержание кальция), чем было раньше. Если коротко: добавление извести повышает рН и выталкивает кальций и бикарбонат из раствора в виде карбоната кальция.
Ограничения
Этот способ очистки воды поможет уменьшить щелочность только в том случае, если присутствует достаточное количество кальция, поскольку он участвует в образовании карбоната кальция. Хотя могут быть внесены изменения в эту процедуру (см. Уменьшение магниевой жесткости), количество магния, которое можно удалить с помощью этого метода, ограничено из-за того, что карбонат магния примерно в 100 раз более растворим, чем карбонат кальция.
С этим методом нельзя уменьшить натрий, так как карбонат натрия очень хорошо растворим в воде. Также не могут быть уменьшены сульфатные и хлоридные анионы. Они останутся неизменными, если не добавляются, хотя добавление солей кальция обычно практикуется для повышения содержания кальция в воде и обеспечения достаточной концентрацией кальция в обработанной воде.
Поскольку щелочность снижается только до тех пор, пока осаждается кальций, важно, чтобы кальциевая жесткость превышала щелочность. Кальциевая жесткость - это другой показатель, характеризующий содержание кальция в воде. Здесь содержание кальция выражается в виде эквивалентного количества CaCO3, вместо количества кальция, который выражается в ppm или мг/л. Чтобы содержание кальция в мг/л или ppm преобразовать как CaCO3 в ppm просто умножьте значение на 2,5.
Например: вода содержит 100 ppm кальция и имеет щелочность 200 ppm в виде CaCO 3. Сколько кальция останется после осаждения щелочности?
Кальциевая жесткость воды в таком случае составит 250 ppm в виде CaCO3. Удаление щелочности 200 ppm в виде мела, также требует уменьшения жесткости кальция на 200 ppm. Оставшаяся жесткость кальция составляет 50 ppm в виде CaСO3 или 20 ppm в виде кальция.
Из-за осаждения кальция может потребоваться добавить в воду еще кальция в виде карбоната кальция или гипса. Это лучше всего сделать до или во время добавления извести. Необходимое количество зависит от предполагаемого осаждения мела и желаемого уровня кальция в воде после обработки.
Весь кальций, который добавляется с известью, также будет осаждаться в виде карбоната кальция. Этот факт обеспечивает соблюдение немецкого закона Reinheitsgebot, поскольку затем ничего не добавляется в воду. На практике этот метод не способен полностью снизить щелочность до 0 независимо от количества присутствующего кальция. Нижний предел снижения щелочности на практике обычно составляет 30-50 ppm в виде CaCO3 . Одна из причин заключается в поглощение атмосферного CO2 в течение времени осаждения, который заставляет часть осаждающегося мела снова раствориться в воде.
Реакция лучше протекает при низких температурах воды, но, в то же время, осаждающийся карбонат кальция образует большие частицы в слегка более теплой воде, поэтому температура обрабатываемой воды не должна быть ниже 12 °C.
Как пользоваться калькулятором
Для очистки воды с использованием извести необходимо рассчитать необходимое количество извести, для этого воспользуйтесь существующей электронной таблицей обработки воды (водный калькулятор.xls).
Вода для предварительной обработки
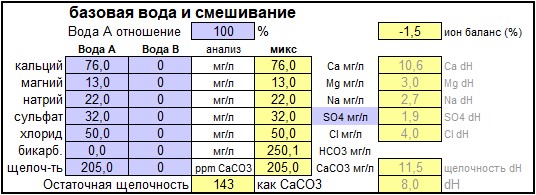
Все расчеты извести сделаны на «расширенном» калькуляторе/электронной таблице. Первый шаг - это ввод профиля исходной воды, который можно взять в полном анализе или GH & KH тесте на воду. У меня есть полный анализ моей воды из колодца, которая очень похожа на воду в Мюнхене. Она обладает высоким уровнем временной жесткости, что хорошо проявляет себя в этом способе обработки, хотя осаждение мела происходит и во время кипячения воды.
 |
Потребность в извести и баланс кальция
Теперь перейдите к разделу «Обработка воды известью». Здесь необходимо указать текущий рН воды и количество воды, подлежащего обработке. РН воды используется для определения количества угольной кислоты и СО 2 в воде. Это необходимо, так как добавленная известь также должна превращать ее в карбонат в дополнение к превращению бикарбоната в карбонат. Количество воды, подлежащей обработке, отличается от общего количества пивоваренной воды, указанной позже, поскольку некоторая вода останется при отделение осадка из обработанной воды.
Результатом расчета является теоретическое количество извести в ppm или мг / л, которое необходимо добавить для осаждения всей щелочности воды. Но более важным результатом, требующим здесь внимания, является избыток кальция. Это количество кальция, который останется в воде, если вся щелочность будет осаждена этим процессом. Если эта концентрация ниже 10 мг/л, вам необходимо добавить некоторые соли кальция (гипс или хлорид кальция), чтобы повысить содержание кальция в воде. В моем случае мне пришлось сделать это, что будет объяснено в следующем разделе.
Есть еще два поля, в которые требуется ввести значения: GH и KH. Это измерения из анализа испытания воды GH & KH, которые берутся из обработанной воды после осаждения карбоната кальция. Поскольку снижение щелочности редко бывает эффективным на 100%, тестирование воды после обработки и использование этой информации вместе с информацией из воды для предварительной обработки является более надежным подходом, чем при произвольной эффективности обработки известью.
Для определения профиля конечной воды предполагается, что обработка известью только осаждала щелочность (например, бикарбонаты и карбонаты) и кальций. Все остальные ионы остаются нетронутыми.
 |
Добавление солей
Возвращаемся к разделу «изменение профиля воды от солей».
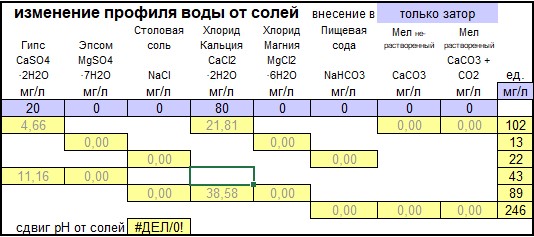
Как упоминалось ранее, используемая здесь вода содержит больше щелочности, чем кальциевая жесткость, которая ограничивает эффективность удаления щелочности и вызывает дефицит кальция в конечной воде. Чтобы этого избежать, я решил повысить уровень кальция в воде с помощью 20 мг/л гипса и 80 мг/л хлорида кальция. При этом повысились уровни содержания кальция, сульфата и хлорида в воде. Их новые концентрации в воде для предварительной обработки можно увидеть в правой колонке.
 |
Потребности в соли и извести для очистки воды
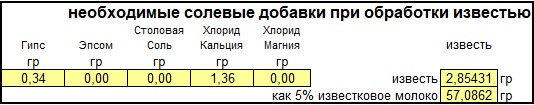
При обработке воды известью добавляются необходимые соли и известь для воды, количество которой больше, чем требуется для пивоварения. Вот почему существует отдельный раздел с названием «Необходимые солевые добавки при обработки известью», который рассчитывает количество солей в пересчете на концентрацию солей и извести, также необходимо знать количество воды для обработки, которое было указанно ранее.
Маловероятно, что пищевая сода добавляется в воду, когда целью является удаления щелочности. Хотя мел может быть добавлен, он добавляется только в качестве вспомогательного средства для процесса и не остается в воде после обработки. Вот почему список солей ограничивается гипсом, солью Эпсома, поваренной солью, хлоридом кальция и хлоридом магния. Необходимое количество извести определяется как для сухого вещества, так и для 5% (по весу) раствора. Последнее полезно для обработки не большего количества воды для тестовых партий, которое будет объяснено ниже.
 |
Полученный профиль воды
Когда значения «GH» и «KH» воды для последующей обработки были введены в разделе «Обработка воды известью», в результате получается профиль воды. Вы заметите, что изменились только кальций и бикарбонаты / щелочность (за исключением ионов, добавленных дополнительными солями). Как упоминалось ранее, в результате предположения, что осаждается только карбонат кальция, поскольку осаждение магния является более сложным.
На этом примере обработка известью понизила остаточную щелочность со 143 ppm до 10 ppm в виде CaCO 3
 |
Оценка pH затора
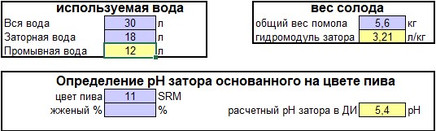
После заливки воды, засыпки помола и определения цвета пива можно оценить рН затора. В моем случае варился Майбок с цветностью 11 SRM, и оценочный рН затора 5.4 был достаточно близок к фактическому рН затора 5.5. Оценка рН менее точная, когда большая часть цвета образуется из базового солода, что было в моем случае.
 |
Что для этого нужно
Чтобы эффективно обрабатывать воду известью, вам понадобятся несколько расходных материалов, некоторые из которых у вас уже есть.
Пищевой гидроксид кальция, а также гашеная известь или гидроокись кальция, можно найти в специализированных магазинах торгующих химреактивами. Если ваши местные магазины не возят его, вы всегда можете заказать его у онлайн-торговцев (например, здесь). Пол килограммовой упаковки хватит на долго.
Осторожно! Гидроксид кальция, также известный как гидратированная или гашеная известь, является агрессивным веществом и с ним следует обращаться с осторожностью. В сочетании с водой, даже влажностью кожи или глаз, она образует каустический раствор, который может вызвать химические ожоги. Храните его в недоступном для детей и домашних животных месте. В дополнение к этому надевайте защитные очки и перчатки всякий раз, когда вы его используете. Проливы следует немедленно вытирать.
Набор для тестирования воды GH & KH - очень полезный инструмент, который позволяет мгновенно проверять результаты очищенной воды. Без средств измерения щелочности вам придется ждать, пока вы не измерите pH затора, чтобы подтвердить успешно ли прошла обработка.
Также необходима большая емкость для обработки воды и выпадения осадка.
Для отмеривания содержания соли и извести необходимы весы с разрешением 0,1 г или меньше.
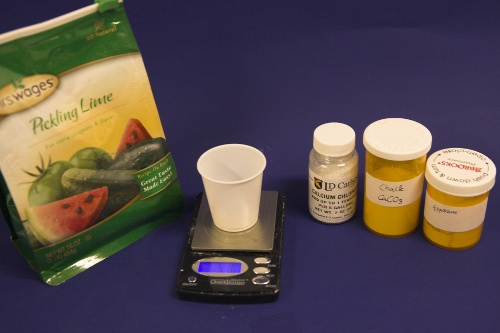 Рисунок 2 - взвешивание количества солей и извести, вычисленных электронной таблицей. Добавьте к этому дополнительно около 1/4 - 1/2 ч.л. мела на каждые 20 л обрабатываемой воды. Нет необходимости быть точным с мелом, поскольку его единственная цель - обеспечить места для кристаллизации осаждающего мела. Добавление мела не обязательно, но полезно Рисунок 2 - взвешивание количества солей и извести, вычисленных электронной таблицей. Добавьте к этому дополнительно около 1/4 - 1/2 ч.л. мела на каждые 20 л обрабатываемой воды. Нет необходимости быть точным с мелом, поскольку его единственная цель - обеспечить места для кристаллизации осаждающего мела. Добавление мела не обязательно, но полезно |
 Рисунок 3 - Заполните большую емкость водой, подлежащей обработке. Для иллюстрации я использовал стеклянный бутыль, но поскольку его вместимость, как правило, меньше, чем количество обрабатываемой воды, он может быть не лучшим выбором. Он также упрощает сифонирование или слив воды после обработки, если емкость помещена достаточно высоко. Рисунок 3 - Заполните большую емкость водой, подлежащей обработке. Для иллюстрации я использовал стеклянный бутыль, но поскольку его вместимость, как правило, меньше, чем количество обрабатываемой воды, он может быть не лучшим выбором. Он также упрощает сифонирование или слив воды после обработки, если емкость помещена достаточно высоко. |
 Рисунок 4 - Добавьте соли, известь и мел в воду Рисунок 4 - Добавьте соли, известь и мел в воду |
 Рисунок 5 - воспользуйтесь миксером, веслом для затирания или просто длинной лопаткой, чтобы хорошо размешать соли, известь и мел в воде. Хоть и вода должна хорошо быть перемешана, но смешивание должно минимизировать поглощение углекислого газа из атмосферы, поскольку он противодействует реакции извести, повышающей рН Рисунок 5 - воспользуйтесь миксером, веслом для затирания или просто длинной лопаткой, чтобы хорошо размешать соли, известь и мел в воде. Хоть и вода должна хорошо быть перемешана, но смешивание должно минимизировать поглощение углекислого газа из атмосферы, поскольку он противодействует реакции извести, повышающей рН |
 Рисунок 6 - Если у вас есть pH-метр или тест-полоски в диапазоне от 8 до 11, вы можете проверить pH после добавления извести. Он должен быть значительно выше 9, но меньше 11. Рисунок 6 - Если у вас есть pH-метр или тест-полоски в диапазоне от 8 до 11, вы можете проверить pH после добавления извести. Он должен быть значительно выше 9, но меньше 11. |
 Рисунок 7 - Пусть осадок оседает в течение ночи Рисунок 7 - Пусть осадок оседает в течение ночи |
 Рисунок 8 - После того, как он будет осажен, pH будет намного ниже, чем после добавления извести, но все же выше, чем было раньше. Но это не проблема, поскольку имеет значение щелочность воды, а не ее рН. На этом этапе вы должны проверить щелочность и жесткость воды и ввести эти измерения в таблицу. Рисунок 8 - После того, как он будет осажен, pH будет намного ниже, чем после добавления извести, но все же выше, чем было раньше. Но это не проблема, поскольку имеет значение щелочность воды, а не ее рН. На этом этапе вы должны проверить щелочность и жесткость воды и ввести эти измерения в таблицу. |
 Рисунок 9 - Слейте очищенную воду с осадка в котел для варки или другую емкость, которую вы используете для нагрева воды Рисунок 9 - Слейте очищенную воду с осадка в котел для варки или другую емкость, которую вы используете для нагрева воды |
Если вы планируете регулярно использовать эту технику на своей пивоварне, предлагаю несколько советов:
- Приобретите большой бак для обработки воды, который будет располагаться в повышенном положении.
- Этот бак должен иметь отвод, достаточно далеко от низа, чтобы не захватывать осадок
- Вы можете спокойно оставить осадок (мел) и остаточную воду в этом баке до следующего раза, когда будете исправлять воду. В этом случае вам не придется добавлять дополнительный мел
- Для того чтобы создать воду со средней остаточной щелочностью между вашей водопроводной водой и самой низкой щелочностью, полученной при помощи известкования, просто смешайте две воды, а не пытайтесь осадить меньше мела. Некоторые эксперименты подтверждают это.
Эксперименты с количеством извести необходимы и актуальны
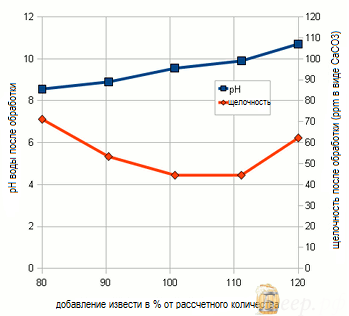 Рисунок 10 - щелочность и рН воды, обработанной известь. Ось X представляет собой известную добавку в процентах от расчетной концентрации
Рисунок 10 - щелочность и рН воды, обработанной известь. Ось X представляет собой известную добавку в процентах от расчетной концентрацииВ результате экспериментов я обнаружил, что количество извести, вычисленное с помощью электронной таблицы, не обязательно является оптимальным количеством, которое дает лучшее снижение щелочности. Это может быть результатом неточностей в данных анализа воды и упрощений, которые были сделаны для расчетов. В результате рекомендуется проверить количество извести в небольшой серии экспериментов, где в воду добавляется различное количества извести и проверяется щелочность полученной воды.
Проведение этих экспериментов довольно прямолинейно. Возьмите воду для предварительной обработки и добавьте соли, чтобы они соответствовали концентрации солей, которые вы планируете использовать для вашей пивоваренной воды. Кроме этих солей добавьте немного мела в воду. Этот мел не раствориться, но даст места для кристаллизации мела, который позже осядет в воде. Не добавляйте известь в этот момент.
Затем разделите эту воду между тремя стеклянными банками (подойдут также стаканы или небольшие колбы). Теперь подсчитайте количество извести, необходимое для осаждения всей щелочности в этих небольших образцах воды. 85% от этой суммы добавьте к первому образцу, 100% добавляйте ко 2-му образцу, и 115% добавьте к третьему образцу. Так как добавленное количество является довольно маленькими, целесообразно приготовить 5 % мас. известкового молока путем простого смешивания 10 г извести с 90 г воды (водопроводная вода будет работать очень хорошо). После доведения до равномерной суспензии количество извести можно измерить с помощью пипетки (1 мл = 0,05 г извести) или путем взвешивания раствора (1 г = 0,05 г извести)
После добавления извести тщательно перемешйте образцы и оставить осадок в течение ночи.
Затем проверьте прозрачную воду на щелочность (KH) и, если возможно, на pH. Я сделал это для 5 различных образцов, и результаты показаны на рисунке 10. По мере увеличения количества добавленной извести оставшаяся щелочность падает до достижения минимума. После этого невозможно осадить дополнительную щелочность. Повышение щелочности после этой точки связано с резким увеличением ионов гидроксида (OH - ), что отражается в повышении рН. Эти остаточные гидроксид-ионы не обнаружили никаких ионов бикарбоната или угольной кислоты.
Для обработки воды следует использовать концентрацию извести, которая ведет к низкой щелочности и приемлемому рН воды (<9,5).
Снижение магниевой жесткости
До сих пор обсуждалось только уменьшение щелочности и кальциевой жесткости, ведь обсуждалось осаждение карбоната кальция. Однако для уменьшения магниевой жесткости также можно использовать обработку воды известью. Повышенные уровня магния вместе с высоким содержанием сульфатов приводят к образованию соли Эпсома, которая может придать горький вкус. Соль Эпсома даже называют Bittersalz (горькой солью) на немецком языке.
Карбонат магния примерно в 100 раз более растворимый, чем карбонат кальция, поэтому он не осаждается, как только повышается концентрация карбоната. Вместо этого магний необходимо осаждать в виде гидроксида магния, который в 100 раз меньше растворим, чем карбонат кальция. Переход из бикарбоната магния в гидроксид магния происходит в этих двух этапах:
- Mg 2+ + 2 HCO 3 - + Ca 2+ + 2 OH - → Mg 2+ + CO 3 2- + CaCO 3 ↓
- Mg 2+ + CO 3 2- + Ca 2+ + 2 OH - → Mg (OH) 2 ↓ + CaCO 3 ↓
Чтобы осадить один ион магния и два бикарбонатных иона, требуется две молекулы гидроксида кальция. Кальций из гидроксида кальция осаждается в виде карбоната кальция вместе с гидроксидом магния.
Чтобы сделать вышеупомянутые реакции, необходимо повысить рН воды до рН 10,5 - 11, что значительно выше рН, необходимого для простого осаждения карбоната кальция. Кроме того, полученная вода будет иметь рН, который останется слишком высоким для использования в качестве пивоваренной воды. Для решения этой проблемы при осаждении магния обычно используют двухступенчатую известковую обработку.
Гидроксид кальция добавляют, примерно, в половину воды для предварительной обработки до достижения рН 10,5-11. После взаимодействия с водой происходит выпадание осадка. Во время этого процесса удаляются как гидроксид магния, так и карбонат кальция. Затем чистая вода отделяется от осадка и смешивается с оставшимся количеством воды для предварительной обработки, что приводит к дополнительному осаждению карбоната кальция, но не осаждает гидроксида магния или карбоната магния. РН воды после обработки на втором этапе будет достаточно низким, для создания подходящей пивоваренной воды.
Такая двухступенчатая очистка воды способна уменьшить содержание магния в воде на 50-65%
Очистка воды на большой пивоварне
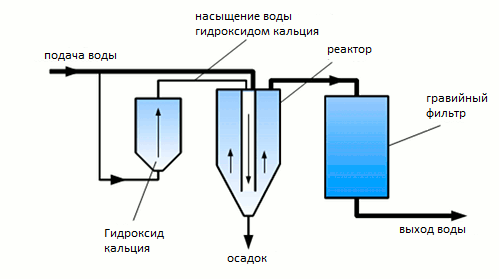 Рисунок 11 - Схематическое изображение простой одноступенчатой системы восстановления щелочности. См. Текст для объяснения
Рисунок 11 - Схематическое изображение простой одноступенчатой системы восстановления щелочности. См. Текст для объясненияМногие пивоваренные заводы проводят обработку воды, обсуждаемую в этой статье, в непрерывных системами. На рисунке 11 показана простая 1-ступенчатая система, которая может быть использована для осаждения карбоната кальция из входящего потока «сырой» воды.
Часть входящей воды отводится в резервуар для хранения гидроксида кальция, где она насыщается гидроксидом кальция. Количество гидроксида кальция, который будет смешиваться с водой, регулируется в зависимости от щелочности, которую нужно осадить. Основной поток воды и насыщенная вода гидроксида кальция тщательно перемешиваются в реакторе. Затем смешанная вода течет по центральной трубе, осаждая карбонат кальция. Как только вода достигает дна, она начинает подниматься вверх, где имеющееся поперечное сечение намного больше, а итоговый поток течет медленнее. Так медленно, что осаждающийся карбонат кальция способен выпадать, а вода, выходящая в верхней части реактора, почти прозрачна. Затем гравийный фильтр удаляет остаточную мутность в воде, и вода, выходящая из системы очистки, прозрачна и имеет низкую щелочность и жесткость, чем вода перед обработкой. Для поддержания работы системы необходимо удалить карбонат кальция в качестве осадка, и в его резервуар для хранения необходимо добавить гидроксид кальция
Современные модификации этой системы используют гранулы карбоната кальция или кварцевый песок (размер зерна 0,2-0,5 мм) в реакторе, которые обеспечивают места кристаллизации карбоната кальция и сокращают время, проведенное в реакторе, до 60-90 мин. Также доступны многоступенчатые установки, способные осаждать магний.
Заключение
Этот метод очистки воды достаточно популярен среди крупных пивоварен, для которых это экономически оправданно при наличии высокой жесткости и щелочности в воде, но редко используются среди домашних пивоваров. Я думаю, что причина этого в некоторой степени очевидна: эта обработка более сложная и менее интуитивная, чем обработка воды кислотами, ее разбавление или даже создание пивоваренной воды с нуля. Тем не менее, этот процесс, безусловно, будет полезен продвинутым домашним пивоварам, и после его создания может стать стандартной процедурой во время приготовления более легких стилей пива, которые требуют более мягкой воды. Даже если это не станет стандартной процедурой, некоторые пивовары смогут просто сказать: были там, сделали это.
|
1. Rush87
2018-04-13, 18:28
|
|
2. Winder
2018-04-16, 19:34
|
|
3. Админ
2018-04-16, 20:10
|
|
4. Winder
2018-04-17, 03:05
|
|
5. Админ
2018-04-17, 08:26
|
|
6. yuruk1985
2018-04-19, 20:15
|
|
7. Админ
2018-04-19, 22:22
|
|
8. yuruk1985
2018-04-20, 06:02
|
|
9. Админ
2018-04-20, 07:37
|
|
10. kolsasha
2018-04-27, 18:52
|
|
11. yuruk1985
2018-04-27, 19:06
|
|
12. kolsasha
2018-04-29, 20:18
|
|
13. yuruk1985
2018-04-29, 21:11
|
|
14. Админ
2018-04-29, 23:39
|
|
15. yuruk1985
2018-05-03, 20:45
|
|
16. yuruk1985
2018-05-03, 20:56
|
|
17. Админ
2018-05-03, 21:22
|
|
18. Angrom
2020-05-30, 10:26
|
